ИСПОЛЬЗОВАНИЕ ИНДИВИДУАЛЬНЫХ ПЛАСТИН В НЕЙРОХИРУРГИЧЕСКОЙ ПРАКТИКЕ
В ветеринарной клинике ЭФА в течение последних 7 лет мы используем, наряду с другими методами, для фиксации тел позвонков индивидуальные пластины. Стабилизация позвоночно-двигательных сегментов представляет определенные сложности, обусловленные особенностями биомеханики и анатомии пораженных и прилегающих к ним позвоночно-двигательных сегментов, что особенно актуально у пациентов со сформированной кифотической и/или сколиотической деформацией позвоночника на фоне спондилитов.
В настоящее время существует множество систем вентральной и дорзальной стабилизации позвоночно-двигательных сегментов, установка многих из них сопровождается травматизацией невральных структур [1–5, 7, 8, 10–16]. Одним из решений данной проблемы может служить применение технологии накостного остеосинтеза с фиксацией соседних позвонков персонифицированными титановыми пластинами, имеющими индивидуальный рельеф прилегающей к кости поверхности и встроенную систему навигации в виде отверстий с предварительно рассчитанными углами наклона, в которые по принципу минимально инвазивного проведения устанавливались винтовые фиксаторы. Пластины производились путем прототипирования на 3D-принтере с применением аддитивных технологий и с учетом особенностей анатомии позвоночно-двигательного сегмента экспериментального животного на основе первичных данных, полученных из пакета DICOM при мультиспиральной компьютерной томографии (МСКТ) пораженного сегмента позвоночника [17–19]. Применение персонифицированных титановых пластин, во-первых, обеспечивает тесное прилегание к любым анатомическим ориентирам и учитывает особенности структуры костной поверхности позвоночника, во-вторых, позволяет вводить винтовые фиксаторы по заранее рассчитанной траектории и существенно снижать риски их мальпозиции с перфорацией позвоночного канала и травматизацией невральных структур. В настоящей статье представлен опыт применения разработанной нами технологии при травматических поражениях позвоночно-двигательных сегментов у собак.
Хирургическое лечение было проведено на 20 животных (собаках разных пород) обоего пола, средний возраст — 3,5 года, средняя масса тела — 32,4 кг, с преимущественно схожим механизмом и последствиями травмы, приведшими к переломовывиху одного из грудных позвонков и грубому неврологическому дефициту по типу центрального парапареза с глубиной неврологических нарушений, оцененной по шкале Frankel [6] от А- до С-степени. Животные получали стандартную послеоперационную терапию и курс реабилитации.
У животных лечение проводилось по следующему плану в соответствии с разработанной технологией:
-Сбор анамнеза и первичное обследование животного, проведение обзорных спондилограмм в прямой и боковой проекциях. Показаниями для проведения МСКТ являлись клинические и рентгенологические признаки нестабильного перелома или переломо-вывиха грудных позвонков.
-Первичное сканирование на МСКТ, формирование пакета данных в DICOM-формате. Обработка техническим специалистом и нейроортопедом полученного пакета данных DICOM и формирование первичного плана хирургического лечения.
-Обработка пакета данных DICOM, создание первичной трехмерной модели поврежденного сегмента позвоночника с разделением на отдельную модель передней опорной колонны (включающую в себя тело, диски и ножки тела поврежденного позвонка) и заднюю опорную колонну (нижние и верхние суставные отростки, поперечные и остистый отростки поврежденного тела позвонка) [4–6].
-Формирование анатомических файлов: восстановленная модель передней опорной колонны, модель задней опорной колонны, формирование модели позвоночника с восстановленным сагиттальным балансом. Утверждение плана хирургического лечения.
-Формирование на 3D-модели проекта виртуально имплантированного в модель набора каналов винтовой фиксации [8] (рис. 1).
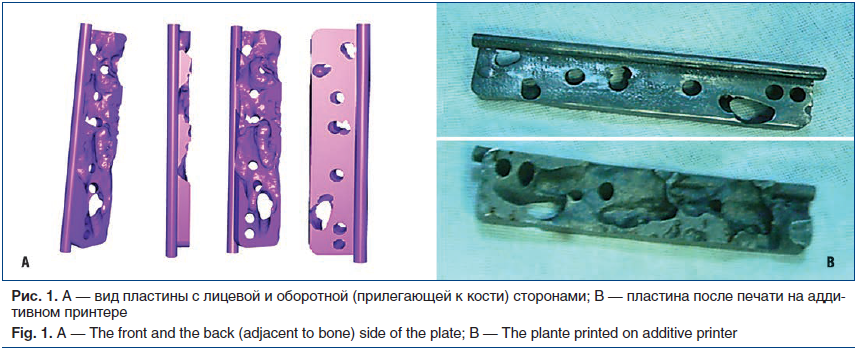

-Печать персонифицированной пластины из пористого титана на 3D-принтере.
-Стерилизация персонифицированной пластины и проведение хирургического вмешательства: задняя декомпрессия спинного мозга методом резекции дужки позвонков (ламинэктомия) с последующим скелетированием участка тел позвонков в месте установки пластины. На подготовленный участок накладывали персонифицированную пластину и фиксировали ее кортикальными винтами, после чего рану закрывали, используя рассасывающийся шовный материал. На кожу накладывали узловатый прерывистый шов из не рассасывающегося материала.
Лечебный мониторинг включал: общий и биохимический анализы крови, рентгенографию и МСКТ позвоночного столба, оценку неврологического дефицита по шкале Frankel.
Статистический анализ проводился на базе программного обеспечения IBM SPSS Statistics 21.0. Количественные данные представлены в виде среднего и стандартного отклонения среднего (М±SD). С учетом небольшого объема совокупности для статистического анализа применяли методы непараметрической статистики. Сравнение результатов контрольной и основной групп проводили с использованием критерия Манна — Уитни для независимых наблюдений, т. к. распределение не соответствовало нормальному, а данные о степени неврологического дефицита на пред- и послеоперационном этапах для каждой из групп сравнивались с помощью критерия Вилкоксона для зависимых наблюдений. Уровень значимости был выбран α=0,05.
Результаты
У животных, по данным рентгенографии и МСКТ (рис. 4) позвоночного столба в послеоперационном периоде, отсутствовало вхождение винтов в позвоночный канал.

Рис.4. Данные МСКТ через 90 дней после установки персонифицированной пластины
Оценку неврологического дефицита по шкале Frankel проводили на 90-е сут после операции и сравнивали с исходными показателями (табл. 1). На дооперационном этапе животные в отношении неврологического дефицита по шкале Frankel распределились на уровнях F.А, F.В, F.С. Наиболее частым нарушением у животных (3 особи) были невральные расстройства в виде дисфункции тазовых органов (задержка мочи), требующие длительного послеоперационного выведения мочи разовым жестким уретральным катетером Нелатона. На 90-е сутки после операции у 2 (20%) особей достигнут максимальный регресс неврологического дефицита (F.E), у 6 (60%) — верифицирована F.D степень, в 2 (20%) случаях установлена F.С степень. Сравнение уровней неврологического дефицита у особей из основной группы на двух этапах выявило статистически значимый (критерий Вилкоксона для зависимых наблюдений T=0,0, p=0,004) его регресс в послеоперационном периоде (90-е сут).
Заключение
Фиксация позвоночно-двигательных сегментов с помощью персонифицированной титановой пластины с навигационными отверстиями позволяет избежать интраоперационной мальпозиции фиксирующих винтов с развитием болевого синдрома и неврологических расстройств; увеличить стабильность фиксации сегментов позвоночника и профилактировать переломы винтов за счет увеличения площади соприкосновения титановой пластины с костью; проводить фиксацию без применения дорогостоящих и потенциально опасных для пациента и персонала систем электронно-оптической рентгеновской визуализации. Полученные результаты позволяют сделать вывод о возможности и целесообразности применения технологии фиксации позвоночно-двигательных сегментов персонифицированными титановыми пластинами с элементами навигации, произведенными на 3D-принтере с применением аддитивных технологий и с учетом особенностей анатомии, в лечении животных.
Оригинальная статья опубликована на сайте РМЖ (Русский медицинский журнал): https://www.rmj.ru/articles/khirurgiya/Ispolyzovanie_additivnyh_tehnologiy_v_personificirovannoy_hirurgii_pozvonochnika_eksperimentalynoe_issledovanie/#ixzz6ZjX2ggdX
Follow us: rusmedjournal on Facebook
